Ley de Joule (Fiz0112)
| Line 1: | Line 1: | ||
| − | ==Ley de Joule== |
+ | ==Máquina Térmica== |
| − | ===Objetivo=== |
+ | ===Objetivos=== |
| − | Estudiar la transferencia de energía desde una resistencia eléctrica al agua, obteniendo a partir de los resultados una medición del equivalente eléctrico del calor. |
+ | - Estudiar el proceso termodinámico realizado por una máquina térmica que es utilizada para elevar una cierta cantidad de masa. |
| + | - Determinar experimentalmente el trabajo realizado por la máquina térmica en base al diagrama P-V. |
||
| − | ===Equipamiento=== |
||
| − | - Computador PC con interfaz PASCO ''Science Workshop'' |
+ | ===Introducción=== |
| − | - Amplificador de Potencia, PASCO CI-6502 |
+ | El propósito de este laboratorio es experimentar con una máquina térmica real, la cual a través de un proceso termodinámico puede hacer un trabajo |
| + | mecánico, elevando pequeñas masas desde una altura a otra. |
||
| − | - Sensor de Temperatura, PASCO CI-6505 |
+ | En esta experiencia se podrá verificar experimentalmente que el trabajo mecánico realizado por la máquina, elevando una masa '''m''' una distancia vertical '''h''', es igual al trabajo termodinámico neto hecho durante el ciclo (área encerrada en un diagrama P-V). Esencialmente, se comparará el trabajo realizado al levantar una masa (<math>W = mgh</math> ), con el trabajo realizado en un ciclo de la máquina térmica como función de la presión y los cambios de volumen. En donde este último está dado por la expresión: |
| − | - Resistencia de <math>10 W</math>, <math>1 W</math> |
+ | :<center><math>W_{neto}=\oint P \cdot dV</math></center> |
| − | - Balanza |
+ | Aunque usted puede demostrar teóricamente ésta relación, la comprobación experimental le permitirá familiarizarse con el funcionamiento de una máquina térmica real. |
| − | - <math>200 ml</math> de agua |
||
| − | - Vaso plástico |
+ | === Experimento === |
| − | - Conectores |
+ | La máquina térmica que se utilizará en este laboratorio, consiste esencialmente de un cilindro plástico con un pistón de grafito en su interior, |
| + | el cual puede moverse a lo largo del cilindro con roce prácticamente despreciable. El pistón está unido a una plataforma mediante una barra |
||
| + | rígida, con el propósito de adecuar el sistema para el levantamiento de masas. Un tubo flexible une la cavidad del cilindro con una cámara de gas, la cual consiste en un cilindro de plomo sellado con un tapón de goma. Esta cámara de gas, con aire en este caso, puede ser ubicada alternativamente en un depósito con agua fría o en un depósito con agua caliente. Una fotografía del montaje experimental de éste levantador de masas es mostrado en la figura 1. |
||
| + | [[File:Lev1.png|center|thumb|600px|]] |
||
| − | ===Teoría=== |
||
| − | El agua es calentada por una resistencia eléctrica sumergida en ella, por la que circula una corriente. El calor disipado por efecto Joule en la resistencia es transferido al agua. Usamos el Principio de Conservación de la Energía, suponiendo que no hay pérdidas de calor, lo que equivale a que toda la energía entregada por la resistencia es absorbida por el agua. |
+ | El ciclo del levantador de masas está representado en la figura 2. Inicialmente el pistón se encuentra el la posición '''a''', aprisionando cierta cantidad de aire en el interior del cilindro. Al poner una masa sobre la plataforma la fuerza sobre el pistón aumenta, ello ocasionando una compresión del aire y por lo tanto un leve descenso del pistón a la posición '''b'''. Si se aumenta la temperatura del gas atrapado dentro del cilindro, el volumen aumentará causando la elevación de la plataforma hasta la posición en '''c'''. Ello se podrá realizar moviendo el |
| + | recipiente desde el depósito frío al depósito caliente. Luego, al remover la masa de la plataforma, la fuerza ejercida sobre el pistón disminuye ocasionando una leve elevación de la plataforma hasta la posición '''d''', ello acompañado de una disminución de la presión de aire en el cilindro. Finalmente el volumen del gas disminuirá cuando la cámara de aire es devuelta al depósito frío, lo que produce el descenso del pistón a su posición original '''a'''. |
||
| + | Para calcular el trabajo termodinámico realizado durante el ciclo, se requerirá dibujar el diagrama P-V. Para ello será necesario determinar los volúmenes y presiones del aire encerrado en el cilindro, tubo y cámara de aire, en los puntos a, b, c y d del ciclo. Por lo tanto previo a ello es necesario encontrar expresiones para: |
||
| − | [[File:Jou1.png|right|thumb|300px| ]] |
+ | :: '''a'''.- El volumen del aire encerrado en el sistema en función de la posición del pistón. Anote el diámetro interno del cilindro como <math>d</math> y la longitud del cilindro ocupada por el gas como <math>L</math>. |
| + | :: '''b'''.- La presión del gas contenido por el pistón de diámetro <math>d</math>. Anote la masa el pistón (más barra y plataforma) como <math>m</math> y la masa agregada como <math>M</math>. No olvide considerar la presión atmosférica (<math>P_0</math>) que actúa sobre el pistón y por lo tanto sobre el gas. |
||
| − | La energía disipada en la resistencia es |
||
| − | :<center><math>E= \bar{P} \cdot t \qquad\qquad\qquad (1)</math></center> |
+ | [[File:Lev2.png|center|thumb|500px|]] |
| − | donde <math>t</math> es el tiempo que circula la corriente y <math>\bar{P}</math> es la potencia promedio, dada por, |
+ | Ahora que se han derivado las ecuaciones básicas necesarias, usted debería ser capaz realizar un ciclo con la máquina térmica, y hacer las mediciones necesarias para calcular el volumen y la presión del aire en los cuatro puntos del ciclo. |
| + | Antes de registrar los datos de la presión, volumen y altura del elevamiento, es recomendable preparar y ejecutar unos pocos ciclos con el propósito de familiarizarse con el sistema. |
||
| − | :<center><math>\bar{P}= \bar{I} \cdot \bar{V} \qquad\qquad\qquad (2)</math></center> |
||
| + | <big><center><FONT COLOR="red">''' ¡Atención! No se debe forzar el pistón. Ello ocasionaría la falla irreparable del sistema.'''</FONT></center></big> |
||
| − | con <math>\bar{I}</math> la corriente promedio y <math>\bar{V}</math> el voltaje promedio. |
||
| − | La energía absorbida por el agua está dada por, |
+ | ==I. Medición del ciclo P-V== |
| − | :<center><math>Q=m \cdot c \cdot \Delta T \qquad\qquad\qquad (3)</math></center> |
+ | ===Equipamiento Requerido=== |
| + | - Máquina de calor/Aparato de Gas Ideal (TD-8572) |
||
| − | donde <math>m</math> es la masa de agua, <math>c</math> es el calor específico del agua (1 cal/gr ºC) y <math>\Delta T</math> es el cambio en la temperatura del agua. Para obtener el equivalente eléctrico del calor, se iguala la energía disipada por la resistencia (en Joule) a la energía ganada por el agua (en calorias). |
+ | - 1 Vaso precipitado de <math>1000 ml</math> (para uso como depósito de agua fría) |
| + | - 1 Vaso precipitado de <math>2000 ml</math> (para uso como depósito de agua caliente) |
||
| − | ===Montaje Experimental=== |
+ | - 1 set de masas de <math>20 gr</math>, <math>50 gr</math>, <math>100 gr</math> y <math>200 gr</math> |
| − | : 1. Pese el vaso plástico. |
+ | - 1 calentador eléctrico de <math>600 W</math> |
| − | |||
| − | : 2. Prepare la resistencia de 10 W, uniendo a ella los conectores aislados necesarios. |
||
| − | : 3. Conecte el Amplificador de Potencia en el Canal C de la interfaz. |
+ | - 1 Termómetro de mercurio |
| − | : 4. Conecte el sensor de temperatura en el Canal A de la interfaz. |
||
| − | : 5. Conecte cables para la medición de voltaje (Sensor de Voltaje) en el Canal B de la interfaz. |
+ | === Procedimiento === |
| − | <center> |
+ | : 1.- Implementar al montaje experimental mostrado en la figura 1. Se deben poner <math>400 ml</math> de agua a temperatura ambiente en el vaso de <math>1000 ml</math>, y en el vaso de <math>2000 ml</math> se deben poner <math>400 ml</math> con agua caliente a una temperatura cercana a <math>70</math>ºC. Esto último se puede lograr poniendo <math>300 ml</math> de agua hirviendo y <math>100 ml</math> de agua de la llave, para hervir el agua utilice el hervidor disponible en el laboratorio. El propósito del calentador eléctrico es mantener la temperatura del agua caliente a <math>70</math>°C. |
| − | {| class="wikitable" border="1" |
||
| − | | '''<u><big>Precaución</big></u>''': <big>asegúrese de que no se produzcan corrientes de aire en el interior del laboratorio, para no alterar las mediciones de la temperatura</big> |
||
| − | |} |
||
| − | </center> |
||
| + | : 2.- Realizar un ciclo completo con la máquina térmica. Se sugiere levantar el pistón unos pocos centímetros antes de cerrar la válvula de entrada del aire (ver figura 1). Note que el aire se filtra fuera del cilindro lentamente, por lo tanto si una masa grande está siendo elevada la filtración aumenta y por ello se sugiere que el límite máximo de la masa agregada en la plataforma de levantamiento sea <math>150 g</math>. Después de observar unos pocos ciclos de la máquina, usted debería ser capaz de describir detalladamente el proceso entre cada uno de los puntos a, b, c y d de un ciclo, indicando cual de las transiciones entre estos puntos son aproximadamente adiabáticas y cuales son isobáricas. Puede observar directamente cambios en el volumen del gas y puede predecir como la presión ejercida sobre el gas por sus alrededores |
||
| + | debería cambiar de un punto a otro usando la definición de presión como fuerza por unidad de área. |
||
| + | : 3.- Tome las mediciones necesarias para determinar el volumen y la presión del aire en el sistema a los cuatro puntos en el ciclo de la máquina (figura 2). Esto se debe hacer rápidamente para evitar escapes de aire alrededor del pistón. Resuma sus resultados en una tabla indicando claramente las unidades de medida. |
||
| − | <center> |
+ | : 4.- Use sus datos para calcular la presión y el volumen del sistema en el los cuatro puntos del ciclo. Escriba detalladamente las ecuaciones y cálculos, sin olvidar las unidades. Recuerde tomar en cuenta el volumen del aire en el tubo y el recipiente de aire. |
| − | {| class="wikitable" border="1" |
||
| − | | '''<u><big>Cuidado</big></u>''': <big>asegúrese que la resistencia esté sumergida en agua cuando conecte el circuito. En caso contrario, ésta se quemará al aplicar el voltaje.</big> |
||
| − | |} |
||
| − | </center> |
||
| + | : 5.- Responda las siguientes preguntas: |
||
| − | : 6. Ponga <math>200 ml</math> de agua en el vaso plástico y péselo. |
+ | ¿Cuál es la altura <math>h</math>, que es elevada la masa? |
| − | : 7. Use agua que esté a unos tres grados por debajo de la temperatura ambiente al iniciar la recolección de datos. |
+ | ¿Podemos sospechar que las transiciones de <math>a \rightarrow b</math> y de <math>c \rightarrow d</math> son aproximadamente adiabáticas? Fundamente su respuesta. |
| − | : 8. Tome datos hasta que la temperatura esté a unos tres grados por sobre la temperatura ambiente. Estas condiciones minimizan efectos del medio, ya que el agua gana energía de éste durante la mitad del experimento y le cede durante la otra mitad. |
+ | ¿Puede demostrar que las transiciones <math>b \rightarrow c</math> y <math>d \rightarrow a</math> son isobáricas? Explique |
| + | porque. |
||
| − | : 9. Reste la masa del vaso, de la masa total, para obtener la masa del agua. Sumerja la resistencia en el agua. Cubra la parte superior del vaso con papel aluminio, para minimizar pérdidas por radiación y convección. |
||
| − | : 10. Encienda el computador y el Amplificador de Potencia. Ponga en ejecución el programa ''Data Studio'' |
||
| − | == Parte I: Calibración del Programa == |
+ | ==II. Cálculo del trabajo termodinámico a partir del diagrama P-V== |
| − | ===Procedimiento=== |
||
| − | : 1. Seleccione el '''Sensor de Temperatura''' para el Canal A, para el Canal B seleccione '''Sensor de Voltaje''' y para el Canal C '''Amplificador de Potencia'''. |
+ | El objetivo de esta sección es dibujar el diagrama P-V para el ciclo en cuestión y determinar el trabajo termodinámico realizado por la máquina. |
| − | : 2. En la ventana del Generador de Señales presione el botón CC y fije el voltaje de salida del Amplificador de Potencia en 9 volt. Presione el botón '''Auto'''. |
+ | : 1.- Dibuje un diagrama P-V para el ciclo de la máquina. Para ello puede utilizar la grilla cuadriculada que se presenta a continuación, o puede generar su gráfico usando un software computacional. |
| − | : 3. En el sensor de voltaje ponga la '''Frecuencia de Muestreo en 10 Hz'''. |
+ | [[File:Lev3.png|center|thumb|600px|]] |
| − | : 4. En '''Opciones (Options)''' seleccione '''Condición de Parada''' e ingrese para el '''Tiempo 10 min'''. En estas condiciones se tomarán 60 datos en los 10 minutos, lo que equivale a un punto cada 10 segundos. Presione aceptar y cierre la ventana. |
+ | : 2.- En el gráfico de la parte a), indique cada uno de los puntos del ciclo (a, b, c y d). Indique sobre el gráfico cual de las trayectorias (<math>a \rightarrow b</math>, <math>b \rightarrow c</math>, etc.) son adiabáticos y cuales son isobáricos. |
| − | : 5. Active la tabla de datos para el canal A. |
+ | : 3.- Encontrar un método para determinar el área encerrada bajo la curva en el diagrama P-V. El área encerrada no cambia mucho si se asume que <math>P</math> es aproximadamente una función lineal de <math>V</math> para las transiciones adiabáticas. Haciendo esta aproximación, la figura es casi un paralelogramo, de tal modo que se puede obtener el área encerrada usando varios métodos. Tres de ellos están listados abajo. Los estudiantes creativos han propuestos métodos aún mejores que estos, por lo tanto usted es libre de proponer otro método. |
| − | : 6. Despliegue la tabla de datos de los canales B y C. |
||
| − | : 7. Presione '''START''' para iniciar la recolección de datos y cierre de inmediato el circuito eléctrico, aplicando el voltaje a la resistencia. |
+ | :: '''Método I''' |
| + | ::: Puesto que la presión no cambia del punto '''b''' al punto '''c''', se puede tomar la presión de esos dos puntos como una presión constante entre los puntos. Lo mismo se mantiene para la transición desde '''d''' hasta '''a'''. De esta manera se obtiene una figura que es aproximadamente un paralelogramo con dos pares de lados paralelos. Puede buscar y aplicar convenientemente la ecuación apropiada para determinar el trabajo termodinámico neto desarrollado. |
||
| − | ==Parte II: Ejecución del Experimento== |
+ | :: '''Método II''' |
| + | ::: Realice el gráfico con una grilla cuadrada y cuente los cuadrados en el área encerrada por las líneas que conectan los puntos a, b, c y d. Luego multiplique por el número de joules que cada bloque representa. Necesitará hacer estimaciones cuidadosas de fracciones de áreas de cuadrados cuando una trayectoria del ciclo corte uno de ellos. |
||
| − | : 1. ''' IMPORTANTE''': mientras se realice la adquisición de datos, agite suavemente el agua, para asegurar calentamiento uniforme. |
+ | :: '''Método III''' |
| − | |||
| − | : 2. Cuando la temperatura alcance un valor tres grados por encima de la ambiente, abra el circuito eléctrico. Continúe agitando el agua y tomando datos. La temperatura subirá hasta un valor máximo, cuando todo el calor de la resistencia se haya disipado, y luego empezará a descender, por disipación al medio. |
||
| − | : 3. Imprima su tabla de datos. |
+ | ::: Tire una línea recta a cada uno de los comienzos y finales de los puntos para las transiciones en el ciclo. Cada ecuación le dará una función que relaciona <math>P</math> y <math>V</math>. Calcule la integral para cada una de estas ecuaciones. |
| − | : 4. Anote las temperaturas máxima y mínima de la tabla, en el rango válido de mediciones. |
||
| − | : 5. Grafique Temperatura vs tiempo. |
+ | :<center><math>\oint P \cdot dV = \int_a^b P \cdot dV + \int_b^c P \cdot dV + \int_c^d P \cdot dV + \int_d^a P \cdot dV </math></center> |
| − | : 6. Para realizar el análisis estadístico presione [[File:Boton2.png|alt=Negrita|link=]] ,seleccione '''Ajuste de Curva''' y '''Ajuste Lineal'''. |
+ | : 4.- Escoja un método para calcular el trabajo termodinámico. Escriba detalladamente los cálculos necesarios y exprese el resultado en joules. |
| − | : 7. Para encontrar el voltaje y la corriente promedios vuelva a la tabla de datos y en los canales B y C presione [[File:Boton2.png|alt=Negrita|link=]] |
+ | : 5.- Calcule el trabajo mecánico realizado por la máquina de calor para elevar la masa. |
| − | : Anote los valores medios de voltaje y corriente que figuran al final de la tabla. |
+ | : 6.- Compare el trabajo termodinámico con el trabajo realizado al elevar la masa. Recuerde usar el número correcto de cifras significativas en su comparación. |
| − | + | : 7.- Escriba sus conclusiones e identifique las posibles fuentes de error. |
|
| − | ===Análisis de Datos=== |
||
| − | |||
| − | : 1. Calcule la Potencia Promedio disipada por la Resistencia, usando la Ec. (2) |
||
| − | |||
| − | : 2. Calcule la Energía (en Joules) disipada por la resistencia durante el tiempo de circulación de la corriente, usando la Ec. (1). |
||
| − | |||
| − | : 3. Calcule la Energía (en calorías) absorbida por el agua usando la Ec. (4). |
||
| − | |||
| − | : 4. Iguale la Energía disipada con la energía absorbida y obtenga a partir de la igualdad, el número de Joules por caloría (equivalente mecánico del calor). Calcule la diferencia porcentual entre el valor medido y el valor aceptado (<math>4,184 J/cal</math>). |
||
| − | |||
| − | : 5. Calcule la pendiente del gráfico <math>T</math>° ''versus'' <math>t</math>. |
||
| − | |||
| − | : 6. Obtenga el equivalente eléctrico del calor a través de la pendiente y compárelo |
||
| − | con el valor aceptado. |
||
| − | |||
| − | |||
| − | ===Preguntas=== |
||
| − | |||
| − | : 1) La energía ganada por el sistema agua-calorímetro resultó ser ¿Mayor o menor que la energía cedida por la resistencia? Explique el resultado. |
||
| − | |||
| − | : 2) La resistencia usada es de <math>1W</math>. ¿Cuánto mayor que este valor fue la potencia característica disipada por la resistencia en el experimento? |
||
| − | |||
| − | : 3) ¿Por que la resistencia no se quemó?. |
||
| − | |||
| − | : 4) ¿Por qué se produce una variación de la intensidad de la corriente y es necesario corregirla? |
||
| − | |||
| − | : 5) ¿Qué error se pretende corregir en la experiencia cuando se le pide que tome un promedio de <math>V</math>?, ¿Por qué puede variar durante el experimento si mantenemos <math>I</math> constante?. |
||
| − | |||
| − | : 6) ¿Qué porcentaje de error tiene el valor de <math>J</math> calculado por Ud., con respecto al valor aceptado?. |
||
| − | |||
| − | : 7) Si Ud. no dispusiera de un voltímetro, ¿que dato adicional necesitaría para calcular <math>J</math>?, ¿Qué inconveniente presenta realizar la experiencia de ésta manera?. |
||
| − | |||
| − | : 8) Indique las posibles fuentes de error en este experimento y como corregirlas y evitarlas. |
||
Revision as of 10:21, 4 March 2014
Contents |
Máquina Térmica
Objetivos
- Estudiar el proceso termodinámico realizado por una máquina térmica que es utilizada para elevar una cierta cantidad de masa.
- Determinar experimentalmente el trabajo realizado por la máquina térmica en base al diagrama P-V.
Introducción
El propósito de este laboratorio es experimentar con una máquina térmica real, la cual a través de un proceso termodinámico puede hacer un trabajo mecánico, elevando pequeñas masas desde una altura a otra.
En esta experiencia se podrá verificar experimentalmente que el trabajo mecánico realizado por la máquina, elevando una masa m una distancia vertical h, es igual al trabajo termodinámico neto hecho durante el ciclo (área encerrada en un diagrama P-V). Esencialmente, se comparará el trabajo realizado al levantar una masa ( ), con el trabajo realizado en un ciclo de la máquina térmica como función de la presión y los cambios de volumen. En donde este último está dado por la expresión:
Aunque usted puede demostrar teóricamente ésta relación, la comprobación experimental le permitirá familiarizarse con el funcionamiento de una máquina térmica real.
Experimento
La máquina térmica que se utilizará en este laboratorio, consiste esencialmente de un cilindro plástico con un pistón de grafito en su interior, el cual puede moverse a lo largo del cilindro con roce prácticamente despreciable. El pistón está unido a una plataforma mediante una barra rígida, con el propósito de adecuar el sistema para el levantamiento de masas. Un tubo flexible une la cavidad del cilindro con una cámara de gas, la cual consiste en un cilindro de plomo sellado con un tapón de goma. Esta cámara de gas, con aire en este caso, puede ser ubicada alternativamente en un depósito con agua fría o en un depósito con agua caliente. Una fotografía del montaje experimental de éste levantador de masas es mostrado en la figura 1.
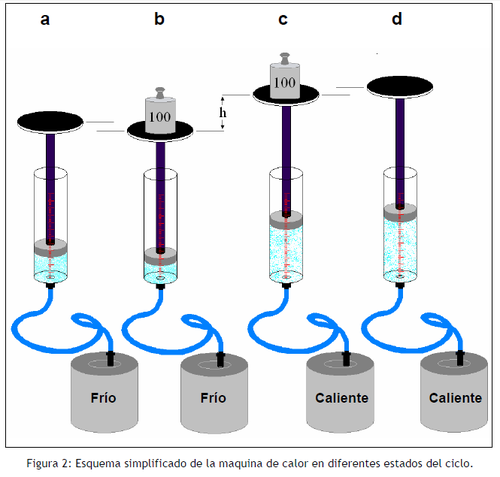
El ciclo del levantador de masas está representado en la figura 2. Inicialmente el pistón se encuentra el la posición a, aprisionando cierta cantidad de aire en el interior del cilindro. Al poner una masa sobre la plataforma la fuerza sobre el pistón aumenta, ello ocasionando una compresión del aire y por lo tanto un leve descenso del pistón a la posición b. Si se aumenta la temperatura del gas atrapado dentro del cilindro, el volumen aumentará causando la elevación de la plataforma hasta la posición en c. Ello se podrá realizar moviendo el
recipiente desde el depósito frío al depósito caliente. Luego, al remover la masa de la plataforma, la fuerza ejercida sobre el pistón disminuye ocasionando una leve elevación de la plataforma hasta la posición d, ello acompañado de una disminución de la presión de aire en el cilindro. Finalmente el volumen del gas disminuirá cuando la cámara de aire es devuelta al depósito frío, lo que produce el descenso del pistón a su posición original a.
Para calcular el trabajo termodinámico realizado durante el ciclo, se requerirá dibujar el diagrama P-V. Para ello será necesario determinar los volúmenes y presiones del aire encerrado en el cilindro, tubo y cámara de aire, en los puntos a, b, c y d del ciclo. Por lo tanto previo a ello es necesario encontrar expresiones para:
- a.- El volumen del aire encerrado en el sistema en función de la posición del pistón. Anote el diámetro interno del cilindro como
y la longitud del cilindro ocupada por el gas como
.
- a.- El volumen del aire encerrado en el sistema en función de la posición del pistón. Anote el diámetro interno del cilindro como
- b.- La presión del gas contenido por el pistón de diámetro
. Anote la masa el pistón (más barra y plataforma) como
y la masa agregada como
. No olvide considerar la presión atmosférica (
) que actúa sobre el pistón y por lo tanto sobre el gas.
- b.- La presión del gas contenido por el pistón de diámetro
Ahora que se han derivado las ecuaciones básicas necesarias, usted debería ser capaz realizar un ciclo con la máquina térmica, y hacer las mediciones necesarias para calcular el volumen y la presión del aire en los cuatro puntos del ciclo.
Antes de registrar los datos de la presión, volumen y altura del elevamiento, es recomendable preparar y ejecutar unos pocos ciclos con el propósito de familiarizarse con el sistema.
I. Medición del ciclo P-V
Equipamiento Requerido
- Máquina de calor/Aparato de Gas Ideal (TD-8572)
- 1 Vaso precipitado de (para uso como depósito de agua fría)
- 1 Vaso precipitado de (para uso como depósito de agua caliente)
- 1 set de masas de ,
,
y
- 1 calentador eléctrico de
- 1 Termómetro de mercurio
Procedimiento
- 1.- Implementar al montaje experimental mostrado en la figura 1. Se deben poner
de agua a temperatura ambiente en el vaso de
, y en el vaso de
se deben poner
con agua caliente a una temperatura cercana a
ºC. Esto último se puede lograr poniendo
de agua hirviendo y
de agua de la llave, para hervir el agua utilice el hervidor disponible en el laboratorio. El propósito del calentador eléctrico es mantener la temperatura del agua caliente a
°C.
- 2.- Realizar un ciclo completo con la máquina térmica. Se sugiere levantar el pistón unos pocos centímetros antes de cerrar la válvula de entrada del aire (ver figura 1). Note que el aire se filtra fuera del cilindro lentamente, por lo tanto si una masa grande está siendo elevada la filtración aumenta y por ello se sugiere que el límite máximo de la masa agregada en la plataforma de levantamiento sea
. Después de observar unos pocos ciclos de la máquina, usted debería ser capaz de describir detalladamente el proceso entre cada uno de los puntos a, b, c y d de un ciclo, indicando cual de las transiciones entre estos puntos son aproximadamente adiabáticas y cuales son isobáricas. Puede observar directamente cambios en el volumen del gas y puede predecir como la presión ejercida sobre el gas por sus alrededores
debería cambiar de un punto a otro usando la definición de presión como fuerza por unidad de área.
- 3.- Tome las mediciones necesarias para determinar el volumen y la presión del aire en el sistema a los cuatro puntos en el ciclo de la máquina (figura 2). Esto se debe hacer rápidamente para evitar escapes de aire alrededor del pistón. Resuma sus resultados en una tabla indicando claramente las unidades de medida.
- 4.- Use sus datos para calcular la presión y el volumen del sistema en el los cuatro puntos del ciclo. Escriba detalladamente las ecuaciones y cálculos, sin olvidar las unidades. Recuerde tomar en cuenta el volumen del aire en el tubo y el recipiente de aire.
- 5.- Responda las siguientes preguntas:
¿Cuál es la altura , que es elevada la masa?
¿Podemos sospechar que las transiciones de y de
son aproximadamente adiabáticas? Fundamente su respuesta.
¿Puede demostrar que las transiciones y
son isobáricas? Explique
porque.
II. Cálculo del trabajo termodinámico a partir del diagrama P-V
El objetivo de esta sección es dibujar el diagrama P-V para el ciclo en cuestión y determinar el trabajo termodinámico realizado por la máquina.
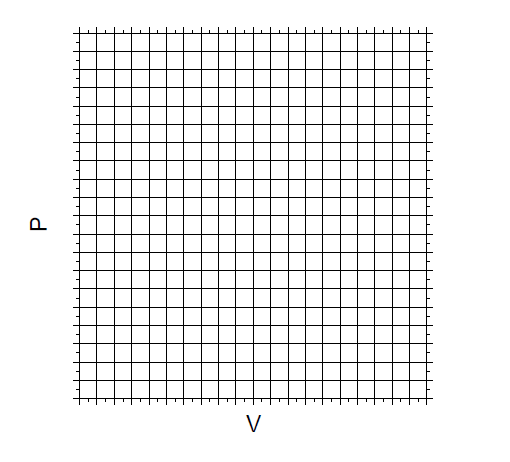
- 1.- Dibuje un diagrama P-V para el ciclo de la máquina. Para ello puede utilizar la grilla cuadriculada que se presenta a continuación, o puede generar su gráfico usando un software computacional.
- 2.- En el gráfico de la parte a), indique cada uno de los puntos del ciclo (a, b, c y d). Indique sobre el gráfico cual de las trayectorias (
,
, etc.) son adiabáticos y cuales son isobáricos.
- 3.- Encontrar un método para determinar el área encerrada bajo la curva en el diagrama P-V. El área encerrada no cambia mucho si se asume que
es aproximadamente una función lineal de
para las transiciones adiabáticas. Haciendo esta aproximación, la figura es casi un paralelogramo, de tal modo que se puede obtener el área encerrada usando varios métodos. Tres de ellos están listados abajo. Los estudiantes creativos han propuestos métodos aún mejores que estos, por lo tanto usted es libre de proponer otro método.
- Método I
- Puesto que la presión no cambia del punto b al punto c, se puede tomar la presión de esos dos puntos como una presión constante entre los puntos. Lo mismo se mantiene para la transición desde d hasta a. De esta manera se obtiene una figura que es aproximadamente un paralelogramo con dos pares de lados paralelos. Puede buscar y aplicar convenientemente la ecuación apropiada para determinar el trabajo termodinámico neto desarrollado.
- Método II
- Realice el gráfico con una grilla cuadrada y cuente los cuadrados en el área encerrada por las líneas que conectan los puntos a, b, c y d. Luego multiplique por el número de joules que cada bloque representa. Necesitará hacer estimaciones cuidadosas de fracciones de áreas de cuadrados cuando una trayectoria del ciclo corte uno de ellos.
- Método III
- Tire una línea recta a cada uno de los comienzos y finales de los puntos para las transiciones en el ciclo. Cada ecuación le dará una función que relaciona
y
. Calcule la integral para cada una de estas ecuaciones.
- Tire una línea recta a cada uno de los comienzos y finales de los puntos para las transiciones en el ciclo. Cada ecuación le dará una función que relaciona
- 4.- Escoja un método para calcular el trabajo termodinámico. Escriba detalladamente los cálculos necesarios y exprese el resultado en joules.
- 5.- Calcule el trabajo mecánico realizado por la máquina de calor para elevar la masa.
- 6.- Compare el trabajo termodinámico con el trabajo realizado al elevar la masa. Recuerde usar el número correcto de cifras significativas en su comparación.
- 7.- Escriba sus conclusiones e identifique las posibles fuentes de error.